近日,我校生命科学与生物制药学院、功能食品与葡萄酒学院及医疗器械学院多学科交叉团队——宋永波/徐慰倬/张景海团队在细胞色素P450酶工程与催化机制研究方面取得重要进展,成功实现了结构多样化甾体的高效、高选择性绿色羟基化。相关研究成果以“Computational Redesign and Mechanistic Insights into P450BM3 Enable Regioselective C−H Hydroxylation of Structurally Diverse Steroids”为题发表于国际催化领域顶级期刊《ACS Catalysis》。
甾体化合物是众多高价值药物的核心骨架,其生物活性高度依赖于特定位置和构型的羟基化修饰。然而,对结构复杂、官能团密集的甾体分子进行高效、精准的区域和立体选择性羟基化,一直是化学合成与生物催化领域的重大挑战。传统化学催化剂常受限于空间位阻和官能团兼容性问题,而天然P450酶虽具催化潜力,但对其非天然底物(如甾体类化合物)往往表现出活性低和选择性差等问题。
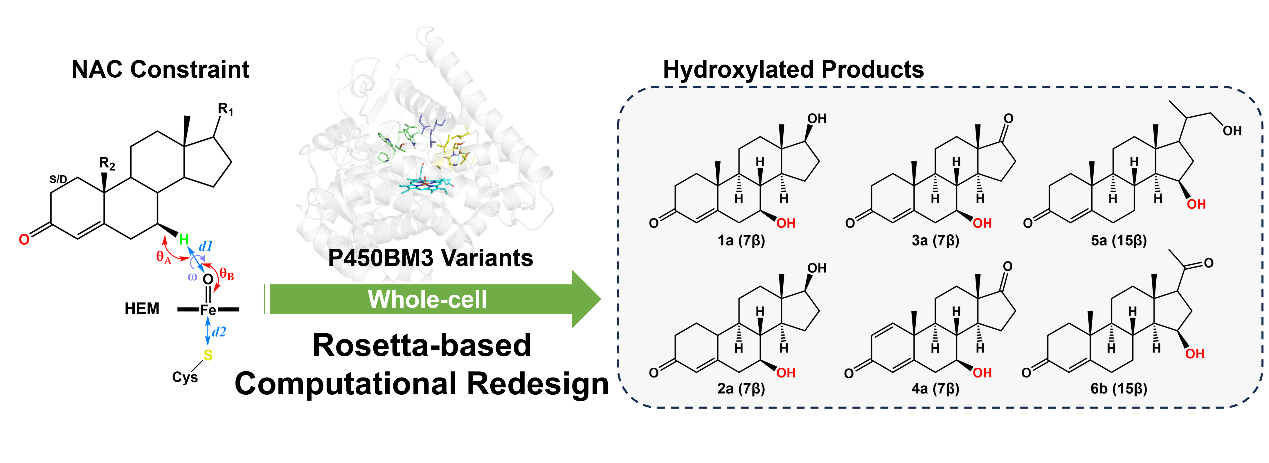
针对这一难题,研究团队创新性地开发了一套“近进攻构象(NAC)”引导的计算-实验一体化工程框架。该策略深度融合Rosetta酶设计、分子动力学(MD)模拟和量子力学/分子力学(QM/MM)计算,成功对P450BM3亲本酶LG23实施精准改造和迭代优化。研究不仅实现了对诺龙、雄二烯二酮等四种小体积甾体95%以上的转化率和超过90%的7β-选择性,更关键的是,通过重塑底物通道(如W330L突变)和调控活性口袋极性(如S88L/T突变),将孕酮等两种含大位阻C17取代基甾体的转化率从不足6%大幅提升至80%以上,并实现了严格的15β-选择性。
在优化的生物转化条件下,团队将雄二烯二酮(ADD)的7β-羟基化产物产量提升至645.4 mg/L,达到目前文献报道的领先水平。更为重要的是,通过深入的机制解析,研究首次揭示了远端残基S88通过一个保守的水分子介导的氢键网络远程调控区域选择性的“分子开关”机制,为P450酶的理性设计提供了普适性的新范式。
该工作不仅为高价值羟基化甾体药物的绿色、高效、规模化生产提供了高性能生物催化剂,所建立的“机制解析–计算设计–实验验证”的循环研究策略也为其他复杂分子的选择性C-H官能化提供了可借鉴的设计蓝图,具有重要的理论意义和广阔的应用前景。
我校2021级博士研究生叶齐为论文的第一作者,宋永波教授、徐慰倬副教授和张景海教授为共同通讯作者,沈阳药科大学为第一通讯单位。该研究获辽宁省科学技术项目以及横向课题等项目的资助。
原文链接: https://doi.org/10.1021/acscatal.5c08382