近日,我校中药学院宋少江教授、刘庆博教授团队在非小细胞肺癌治疗研究领域取得新进展。相关研究成果以“Identification of HMGB1 as a target of 3-O-benzoyl-20-deoxyingenol in NSCLC therapy using integrated ABPP and SIP”为题,发表在期刊《Acta Pharmaceutica Sinica B》上。

目前,非小细胞肺癌(NSCLC)约占肺部恶性肿瘤的85%,其临床治疗长期受制于高复发率、易转移及耐药性等问题,整体远期疗效并不理想。面对这些临床难题,研发新型小分子靶向药物已成为迫切需求。
本研究从甘遂中鉴定出天然活性小分子3-O-苯甲酰基-20-去氧巨大戟萜醇(3-Bz-20-DOI),该化合物可显著抑制非小细胞肺癌(NSCLC)细胞增殖,且细胞毒性较低。通过整合活性基化学蛋白质组学(ABPP)与结构相互作用组学(SIP)的策略,我们证实3-Bz-20-DOI能够特异性靶向HMGB1蛋白。值得注意的是,甘草的主要活性成分甘草酸(GA)能通过HMGB1途径拮抗3-Bz-20-DOI对HMGB1的调控作用,这揭示了甘草与甘遂在“中药十八反”中相互抵消疗效的分子机制。
综上,本研究证实靶向HMGB1是NSCLC治疗的有效策略,为后续开发新型靶向药物提供了关键理论依据。
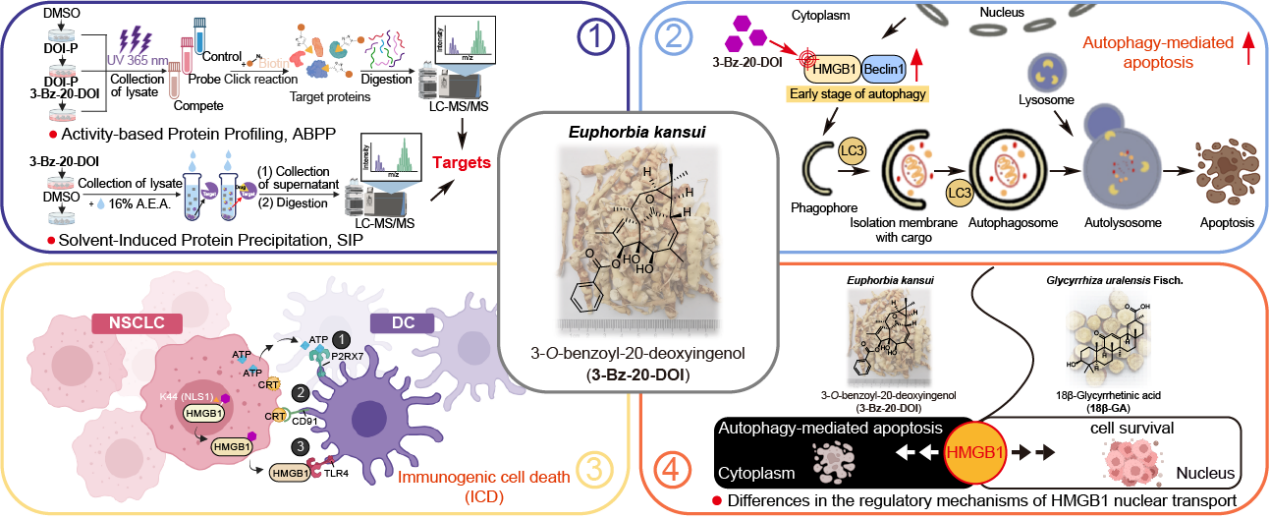
具体研究内容如下:
1、整合ABPP和SIP策略发现HMGB1是3-Bz-20-DOI抗NSCLC的关键靶标。
体内外实验显示3-Bz-20-DOI具有显著的抗NSCLC活性,且毒性远低于顺铂。为鉴定3-Bz-20-DOI的抗NSCLC作用靶标,本研究合成了与3-Bz-20-DOI具有相似活性和高标记效率的光亲和探针DOI-P,并整合ABPP和SIP策略发现3-Bz-20-DOI抗NSCLC作用的关键靶标为HMGB1。这一分析结果在CETSA、SIP、DARTS及Pull-down等实验中均得以证实。
2、3-Bz-20-DOI通过结合HMGB1核定位序列NLS1中的第44位赖氨酸残基来抑制HMGB1核移位,并促进HMGB1与Beclin1结合,最终诱导NSCLC细胞发生自噬介导的细胞凋亡和免疫原性细胞死亡。
为进一步阐明3-Bz-20-DOI的药理学机制,本研究纯化了HMGB1蛋白(全长、A-box和B-box结构域),利用凝胶标记实验确定主要结合区域为A-box结构域,随后通过分子对接、分子动力学模拟等手段初步预测其结合方式,最终通过点突变、BLI和ITC等方式确证3-Bz-20-DOI与HMGB1的结合位点为第27位组氨酸和第44位赖氨酸。值得注意的是,HMGB1中的第44位赖氨酸位于HMGB1的核定位序列NLS1中,该位点的突变会抑制HMGB1核移位,在本研究中发现,3-Bz-20-DOI对HMGB1(K44A)的调控作用相较于HMGB1(WT)会显著减弱,这也从侧面证明3-Bz-20-DOI主要结合该位点来抑制HMGB1的核移位。全蛋白质组学分析和充分的实验证据表明,3-Bz-20-DOI通过促进HMGB1与Beclin1相互作用激活早期自噬,最终诱导NSCLC细胞发生自噬介导的细胞凋亡和免疫原性细胞死亡。
研究创新性地整合了标记(如基于活性的蛋白质组分析,ABPP)与非标记(如溶剂诱导沉淀法,SIP)靶点鉴定策略,明确了中药甘遂中活性成分3-Bz-20-DOI抗非小细胞肺癌的直接作用靶标为HMGB1。在此基础上,首次在靶点层面阐明了“中药十八反”中甘草与甘遂相互抵消疗效的分子机制,为理解中药配伍禁忌提供了新的分子视角。
沈阳药科大学中药学院天然药物化学专业博士研究生王亚旭为论文的第一作者,沈阳药科大学中药学院宋少江教授和刘庆博教授,中国中医科学院青蒿素研究中心王继刚研究员,谷丽维副研究员,为文章的通讯作者,沈阳药科大学为第一通讯单位。
原文链接:https://doi.org/10.1016/j.apsb.2026.01.043