近日,药剂领域知名期刊Journal of Controlled Release《控制释放杂志》(IF=11.5,Q1)在线发表了我校毛世瑞教授团队的最新研究成果“An inhalable liquid-core lipid nanoplatform enables macrophage-mediated mRNA delivery to lung tumors”(cover story),报道了一种吸入式可变形纳米粒,借“巨噬细胞之舟”精准打击肺癌。
肺癌是全球范围内发病率和死亡率最高的恶性肿瘤之一。 目前,以手术、化学疗法及放射疗法为代表的常规治疗策略已步入平台期, 存在难以清除癌细胞的瓶颈。 尽管免疫疗法极大地改变了晚期非小细胞肺癌 (NSCLC) 患者的治疗模式,但整体客观缓解率仅在 10%—30% 之间,面临响应率低的难题。随着对肺癌分子生物学的深入研究和核酸药物的临床使用,基因免疫疗法通过纠正驱动肿瘤的异常基因以调动机体自身免疫系统来清除肿瘤细胞,为肺癌患者点燃新希望。
肺癌基因治疗成功的关键是外源基因在目的细胞中高效且稳定的表达。 然而,实体瘤内较高的间质液压力及致密的细胞外基质导致核酸药物难以递送到肺部肿瘤部位且转染效率低。 申请人所在团队前期研究发现,与针对肺癌细胞的基因递送相比, 基于肿瘤相关巨噬细胞 (TAMs) 靶向策略的吸入式 mRNA 疗法可通过调动机体自身免疫系统识别并清除肿瘤细胞。然而进一步预实验则发现,撤药后,TAMs 的表型和功能极易恢复到调控前的 M2 样免疫抑制状态。 此外, TAMs 作为信息中心,通过抗原提呈促进肿瘤浸润 T 细胞从前体耗竭状态分化为终末耗竭状态, 导致癌症-免疫循环难以在肺部肿瘤部位激活,难以产生长效抗肿瘤免疫。
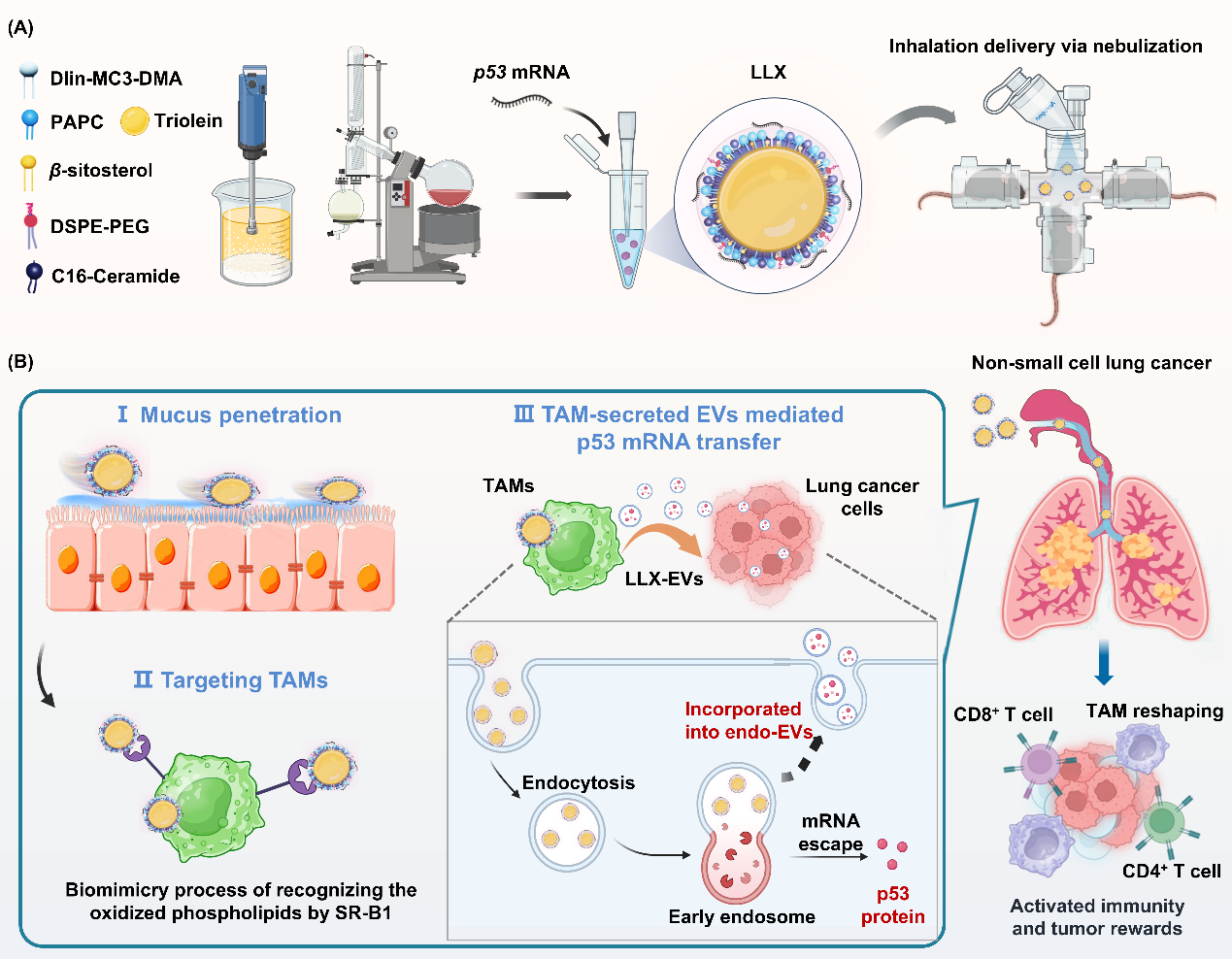
基于上述背景, 针对核酸药物难以递送到实体肿瘤部位且转染效率低,以及癌症-免疫循环难以在免疫抑制微环境中激活的瓶颈问题, 本课题另辟蹊径,通 过 构 建 吸 入 式 液 态 核 心 脂 质 纳 米 递 送 平 台 (mRNA-nLNPs) 调 控“TAMs-NSCLC 细胞-T 细胞”的直接相互作用,在对 TAMs 重编程的同时补偿NSCLC 细胞中抑癌基因的表达、抑制耗竭前体 T 细胞终末分化,以激活癌症-免疫循环进而实现持续的肿瘤消退。雾化给药后, mRNA-nLNPs 的液态核心赋予其高形变能力,以顺利穿过黏液屏障。通过模拟 TAMs 清道夫受体识别羧化磷脂的仿生过程, mRNA-nLNPs 特异性地靶向 TAMs。通过引入锥形结构的辅助脂质 C16-酰胺, mRNA-nLNPs 能够扰乱内体膜结构并促进外源性 mRNA 装载于外泌体 (EVs) 囊泡中分泌。利用内源性 EVs 介导的细胞间 RNA 转移特性,“接力式”将 mRNA 药物递送至 NSCLC 细胞,从而绕开实体瘤微环境对纳米粒子被动扩散的阻碍和尺寸的限制。 本课题提出了与传统依赖纳米粒子被动扩散截然不同的核酸药物实体瘤递送新机制,有望最大程度激活免疫, 助推肺癌及其他肺部疾病的基因治疗。
我校师资博士后刘畅为论文的第一作者,毛世瑞教授为本文的通讯作者,沈阳药科大学为第一通讯单位。
文章链接: https://doi.org/10.1016/j.jconrel.2026.114601