在肿瘤原位疫苗(in situ cancer nanovaccine)研究中,如何高效捕获肿瘤细胞死亡后释放的内源性抗原,并同时克服肿瘤免疫抑制微环境,是制约疗效提升的关键瓶颈。针对这一问题,沈阳药科大学无涯创新学院王永军团队设计了一种“没食子酰介导抗原捕获 + 缺氧响应免疫重编程”协同策略,构建了多功能脂质体纳米平台L-GA/INC/PPa,实现了光动力治疗(PDT)诱导抗原释放、广谱抗原捕获以及免疫抑制逆转的协同增效。该研究发表于ACS Nano(IF=16.1,中科院一区)。
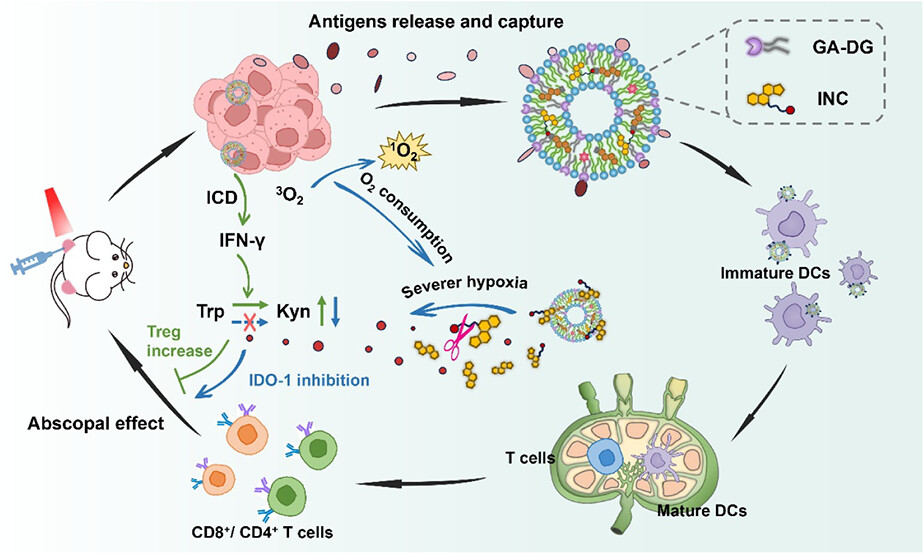
该平台以没食子酸(GA)的多酚-蛋白相互作用为基础,在脂质体表面引入没食子酰基用于非共价抗原捕获;同时加载光敏剂 PPa 诱导免疫原性细胞死亡(ICD),并共载缺氧激活型 IDO-1 抑制剂前药(INC)。在激光照射后,体系可形成“PDT释放抗原/DAMPs → 表面广谱捕获 → 缺氧激活免疫调控”的连续过程,从而增强抗肿瘤免疫应答。
该工作的核心优势与研究发现:
(1)广谱抗原捕获,激发更强免疫应答:与传统的基于马来酰亚胺的共价结合策略相比,没食子酰基化脂质体展现出更卓越的抗原捕获能力。蛋白质组学分析显示,它能捕获多达742种蛋白质,其中包括15种新抗原和多种关键DAMPs,种类比马来酰亚胺修饰组多出239种。这种广谱捕获能力确保了抗原结构的完整性,并显著促进了树突状细胞的成熟、抗原交叉呈递以及效应T细胞的浸润。
(2)协同增效,双重调控肿瘤微环境:该平台不仅通过PDT诱导免疫原性细胞死亡(ICD),释放大量抗原;同时,PDT过程加剧的肿瘤乏氧环境精准激活了共载的IDO-1抑制剂前药(INC),在肿瘤局部释放活性抑制剂,有效逆转了由IDO-1介导的调节性T细胞(Treg)扩增,从而缓解了肿瘤微环境的免疫抑制。
(3)强效抑制原发与远端肿瘤,激发“远端效应”:在B16-F10黑色素瘤小鼠模型中,L-GA/INC/PPa结合PDT治疗展现出了优异的抗肿瘤效果。特别是在双侧荷瘤模型中,该策略与PD-1/PD-L1抑制剂(BMS-202)联用,不仅显著抑制了原发肿瘤的生长,还对未经照射的远端肿瘤产生了强大的“远端效应”。其机制在于,该疗法系统性增强了肿瘤引流淋巴结中DC的成熟与迁移,并显著提升了CD8+ T细胞在远端肿瘤中的浸润,同时减少了Treg细胞的比例。
(4)安全性良好,具备转化潜力:初步的生物安全性评估显示,L-GA/INC/PPa治疗组的小鼠体重稳定,主要器官未见明显病理损伤,肝肾功能指标维持在正常范围内,显示出良好的生物相容性和安全性。
该研究提出了一种面向原位肿瘤疫苗的新型平台化思路:以没食子酰化脂质体为核心,兼顾抗原捕获广谱性、抗原完整性保护和肿瘤免疫抑制逆转,显著提升 PDT 基础上的光免疫治疗效能。研究结果表明,该策略有望为个体化肿瘤免疫治疗和原位疫苗设计提供新的材料与机制学依据。
2020级博士研究生叶剑英为论文第一作者,博士后于江、刘洪卓教授、王永军教授为论文共同通讯作者,沈阳药科大学为第一通讯单位。该研究得到了国家自然科学基金(No. 82273878, 82473872)等项目的资助。
原文链接:https://doi.org/10.1021/acsnano.5c18030