在肿瘤治疗和精准药物递送领域,靶向纳米载体因其高选择性和疗效潜力而备受期待。然而,蛋白冠效应会掩盖表面修饰的配体,导致靶向性丧失;同时,传统的抗体化学偶联工艺复杂,存在免疫原性风险和产业化障碍。这些瓶颈长期阻碍了主动靶向纳米药物的临床转化。近日,沈阳药科大学无涯创新学院王永军教授团队在Nature Communications(IF=15.7)发表研究成果,报道了一种基于没食子酰基修饰脂质的表面没食子酰基化脂质体(Galloylated liposomes, GA-lipo)。该体系通过非共价方式稳定吸附抗体,实现抗体Fab端定向暴露,且不受蛋白冠遮蔽影响,在动物模型中验证了该策略的高效靶向递送和显著抗肿瘤疗效。
团队首先合成并筛选了一系列没食子酰基修饰脂质(GA-lipids),将其掺入脂质体双分子层中,构建了具有表面没食子酰基化特征的 GA-lipo。实验表明,该脂质体表面暴露的没食子酰基团能够通过氢键、疏水作用和静电作用高效吸附多种蛋白质,包括抗体、转铁蛋白等,并在不同pH和血浆环境下保持稳定结合。进一步研究显示,GA-lipo与抗体(如曲妥珠单抗)的结合主要发生在抗体 Fc 区,从而使 Fab 区自然朝外暴露。这种空间取向保证了即使在蛋白冠形成后,抗体的识别能力依然保持。分子动力学模拟揭示了Fc-没食子酸之间由疏水作用和氢键驱动的优先结合机制。在应用层面,研究团队将临床ADC药物Enhertu的有效成分DXd衍生物(DXdd)远程负载至 GA-lipo 中,获得了高达95%的包封率,每个抗体可携带约580个药物分子。在小鼠 HER2 阳性肿瘤模型中,曲妥珠单抗修饰的 GA-lipo(T@GA-DX-lipo)表现出显著优于传统偶联脂质体和未修饰对照的抗肿瘤效果,且降低了肝脾蓄积和系统毒性。
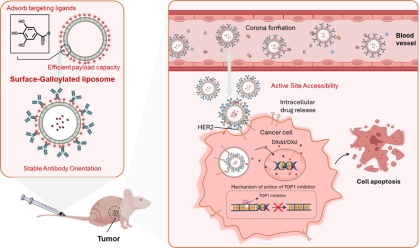
图1 GA-lipo能稳定吸附靶向抗体,并在蛋白冠形成下保持Fab端暴露,实现曲妥珠单抗介导的精准药物递送
该工作提出了一种全新的“没食子酰基化脂质体–抗体预吸附”策略,突破了蛋白冠效应这一制约靶向纳米药物临床转化的核心难题。通过简化工艺、提高稳定性和保证靶向功能,该体系为构建下一代精准纳米药物递送系统提供了可行路径,有望扩展应用于各种疾病治疗精准递送场景。具有以下研究亮点:
1. 简洁的构建方式:在温和条件下实现抗体非共价吸附,避免了传统化学偶联带来的复杂工艺和免疫原性风险;
2. 稳定吸附与功能保持:抗体在蛋白冠形成后仍保持Fab区暴露,确保了靶向功能不受干扰;
3. 广泛适配性与临床潜力:除曲妥珠单抗外,GA-lipo 还可稳定吸附西妥昔单抗、利妥昔单抗等多种单抗,显示出平台化和普适性。其简便、可规模化的特征为抗体修饰纳米药物的开发和产业化提供了新范式。
2022级博士研究生李金菠和博士后于江为论文共同第一作者,刘洪卓教授、刘丹教授、王永军教授为本文共同通讯作者,沈阳药科大学为第一通讯单位。该研究得到了国家自然科学基金(No. 82273878和No.82473872)和沈阳市自然科学基金(No. 23-503-6-11)的资助。
原文链接:https://doi.org/10.1038/s41467-025-63198-4