近日(12.25.2024 Online),药物化学学科国际顶级期刊Journal of Medicinal Chemistry(IF = 6.8)在线发表了我校翟鑫教授课题组在ATX抑制剂治疗肺纤维化领域取得的最新研究成果,论文题目为“Discovery of Novel 4,5,6,7-tetrahydro-7H-pyrazolo[3,4-c]pyridin-7-one Derivatives as Orally Efficacious ATX Allosteric Inhibitors for the Treatment of Pulmonary Fibrosis”。
肺纤维化(PF),是一种进行性、致命性的肺部疾病,且目前缺乏有效的治疗手段。自分泌运动因子(ATX)催化溶血磷脂酰胆碱(LPC)水解为具有生物活性的溶血磷脂酸(LPA)并释放出胆碱的过程在肺纤维化的发生和发展过程中发挥着重要作用。课题组多年以来致力于以ATX为靶标的抗肺纤维化创新药物的研究,积累了丰富的成果和经验。
课题组以处于II期临床研究的ATX抑制剂PAT-409为先导化合物,运用局部修饰和骨架跃迁等策略,结合计算机辅助药物设计,获得了一系列以4,5,6,7-四氢-7H-吡唑并[3,4-c]哌啶-7-酮为核心骨架的新型ATX变构抑制剂。经过广泛的构效关系研究和渐进的结构衍化,得到了优选化合物31和35,对ATX表现出强的抑制活性,IC50分别为2.8nM和0.7nM。QikProp计算结果显示,这两个化合物均具有良好的ADMET特性(#star = 0)。
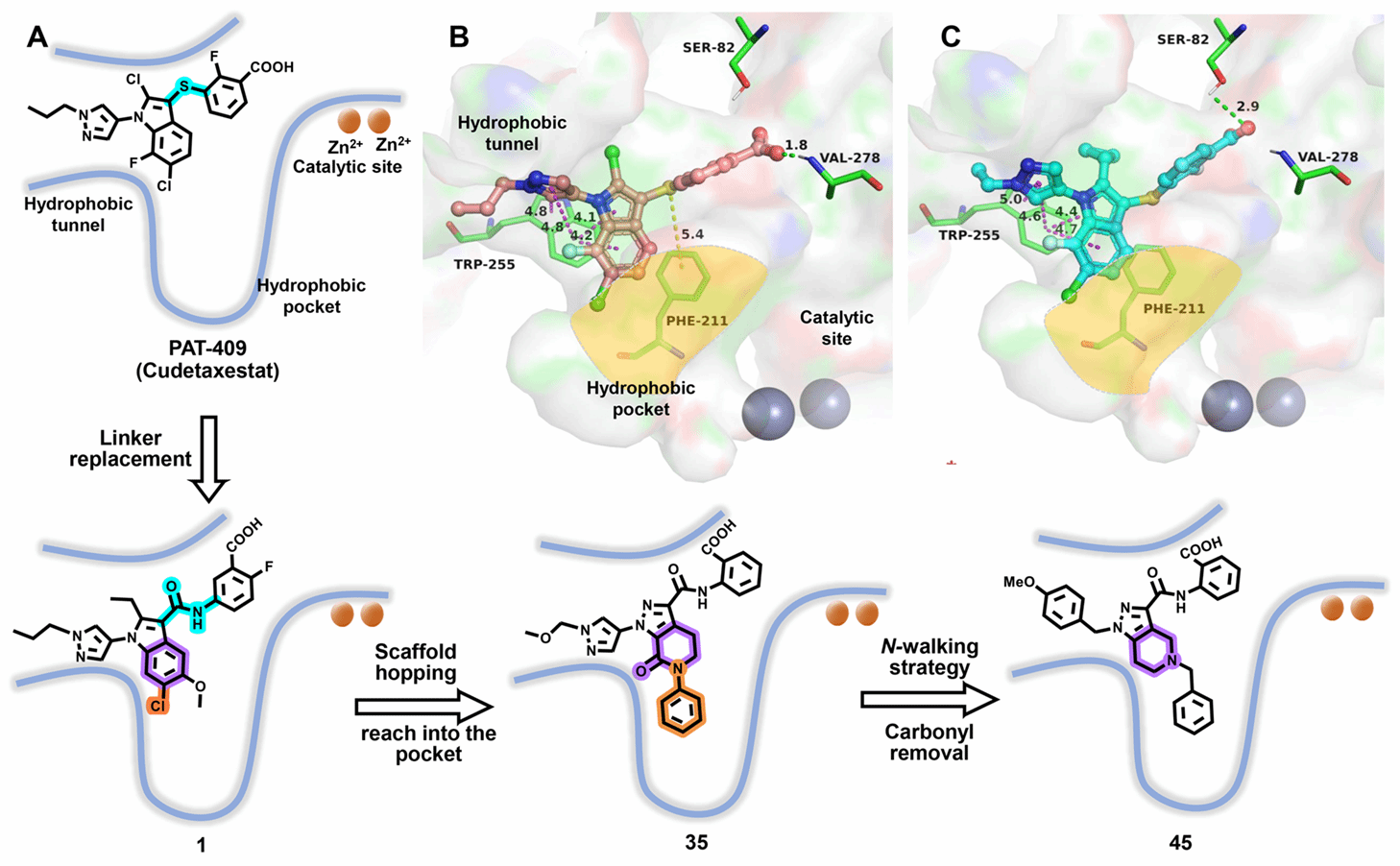
图1.合理的药物设计
在人体胚胎肺成纤维细胞MRC-5中,化合物31和35能够显著抑制TGF-β1诱导的细胞迁移,并降低纤维化相关的基因(α-SMA、COL1A1、FN)的表达。肝微粒体研究表明,化合物31和35具有良好的代谢稳定性(t1/2 > 96 min, CLint < 14.5 µL/min/mg)。体内药代动力学研究发现,化合物35的药动学性质良好,半衰期为1.6 h,口服生物利用度为69.5%。
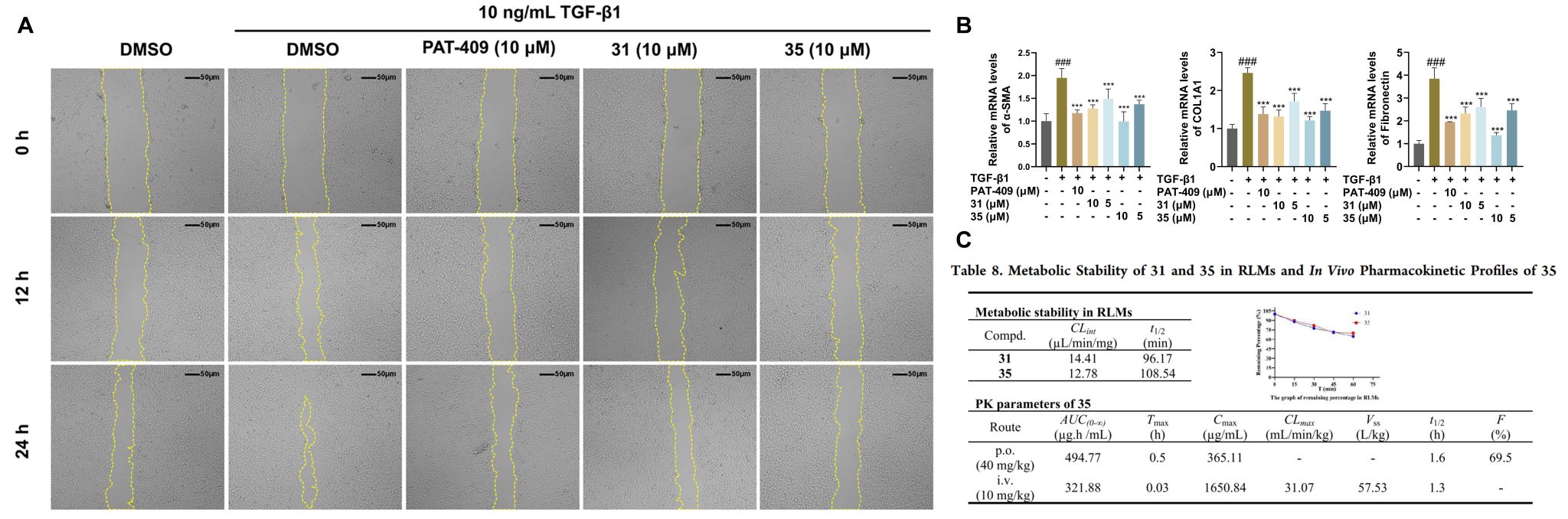
图2.部分体外药理实验结果和体内药动学实验结果。(A)化合物31和35显著抑制TGF-β1诱导的细胞迁移;(B)化合物31和35降低纤维化相关的基因的表达;(C)肝微粒体和药动学实验结果
体内药效学研究表明,化合物31和35以60 mg/kg剂量给药能够显著抑制博来霉素诱导的肺纤维化发展。分子机制研究表明,化合物35能有效降低肺组织中p-Smad2和p-Smad3的上调,证实其通过调节TGF-β/Smad信号通路来发挥抗肺纤维化作用。
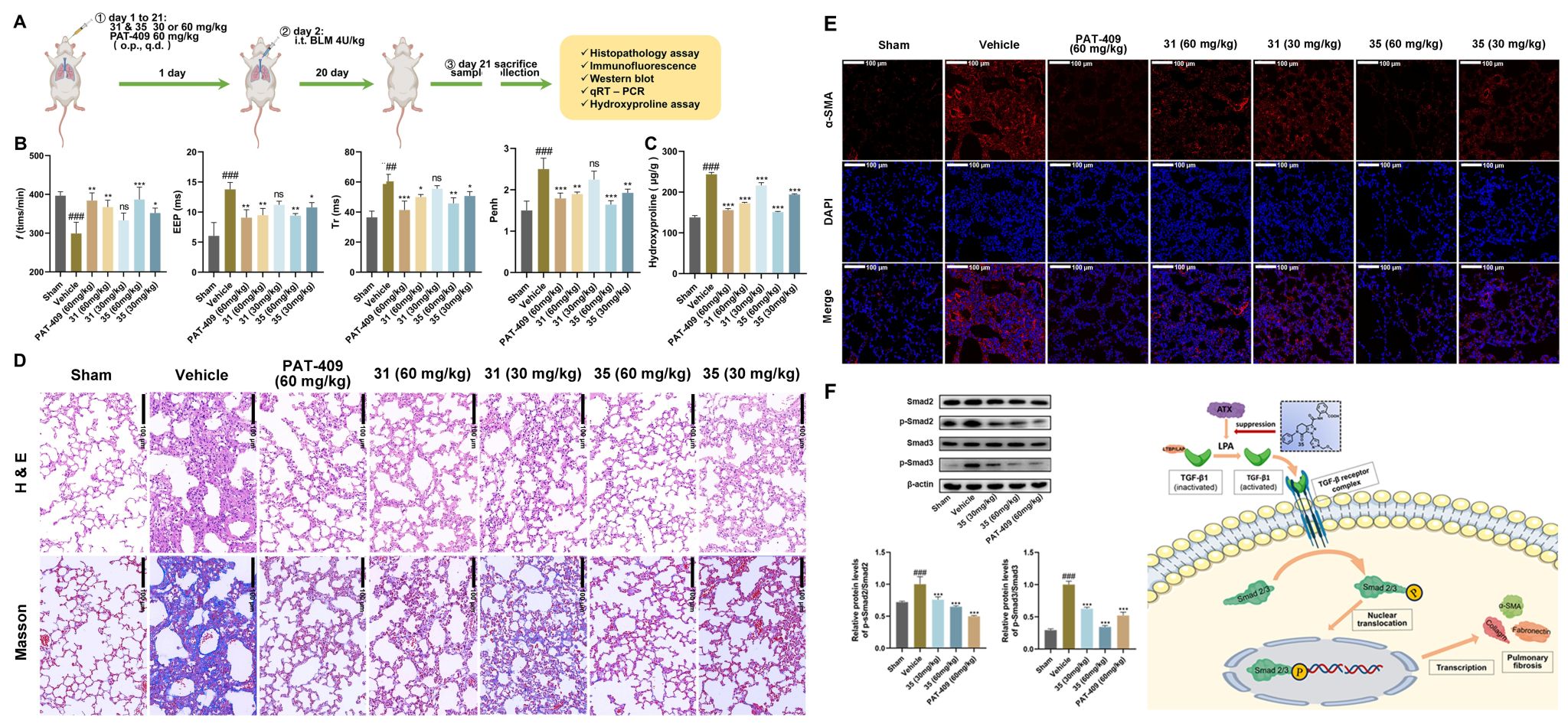
图3.部分体内药效学实验结果. (A) 体内药效学实验方案;(B)呼吸窘迫相关参数;(C)肺组织羟脯胺酸含量检测;(D)肺组织H/E和Masson染色;(E)肺组织α-SMA免疫荧光检测;(F)机制研究
在安全性方面,通过hERG实验证明了化合物35的心脏安全性。通过体内药效学研究过程中各组小鼠的体重变化以及治疗后主要器官的H&E染色结果证明了给药剂量下各化合物的良好体内安全性。
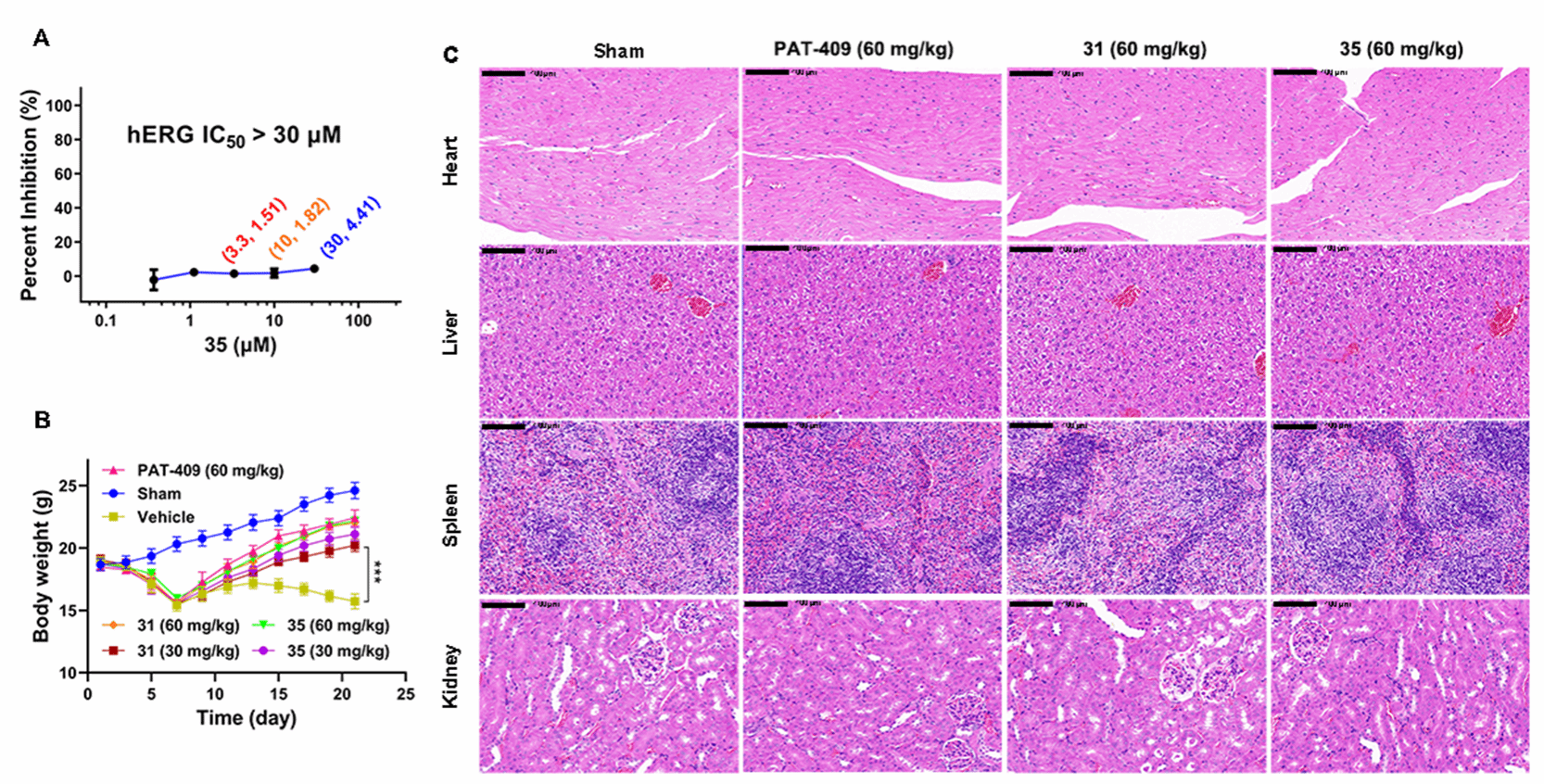
图4.安全性评估结果
我校2021级药物化学专业博士研究生马德翊和师资博士后谭泽晖为论文共同第一作者,制药工程学院翟鑫教授和类红瑞特聘教授为共同通讯作者。该研究工作得到了国家自然科学基金面上及青年项目的资助。
文章DOI: https://doi.org/10.1021/acs.jmedchem.4c02719