小胶质细胞过度活化介导的神经炎症与神经退行性疾病(NDDs)的发生发展密切相关,寻找天然来源的神经炎症抑制剂已成为开发抗NDDs药物的重要策略之一。近年来,生物碱类化合物因其显著的中枢神经系统作用而备受关注,但因其分离难度大、异构体众多,绝对构型确证困难等原因,限制了深入的生物活性评价。如何有效的分离纯化该类天然产物,综合运用多种谱学手段结合计算机辅助计算确证其立体构型,是我们一直在探索解决的问题。近日,李宁教授课题组以白药子中的异喹啉类生物碱存在的氮醛基异构化现象为例,通过NMR谱图分析、手性拆分结合计算ECD方法以及基于TDDFT理论的构象转化能量计算解决化合物的立体异构化问题,在该研究领域取得了新突破(J. Nat. Prod., 2020, DOI: org/10.1021/acs.jnatprod.9b00483)。
李宁教授课题组在发现和寻找天然来源的神经炎症抑制剂方面做了一系列的工作(J. Nat. Prod.,2019,82, 2238-2245;J. Nat. Prod.,2017,80, 3081-3092;Bioorg. Chem.,2020,97, 103690;Phytomedicine,2018,40, 10-19;Sci. Rep.,2017,7, 13608)。建立了LPS诱导的小胶质细胞N9或BV2体外评价模型和LPS、Aβ、喹啉酸、缺血等所致NDDs体内模型,系统评价天然产物体内外抗神经炎症活性,形成了中药防治神经退行性疾病的物质基础和作用机制评价体系,快速发现天然来源神经炎症抑制剂先导化合物。
在前期工作基础上,作者筛选发现传统中药白药子(Stephania cepharantha)总生物碱表现出显著的体外抗神经炎症活性(IC50,1.8±2.2mg/mL),活性追踪分离得到8个异喹啉类生物碱,包括6个新化合物和2个已知化合物(Figure 1,J. Nat. Prod., DOI: org/10.1021/acs.jnatprod.9b00483)。
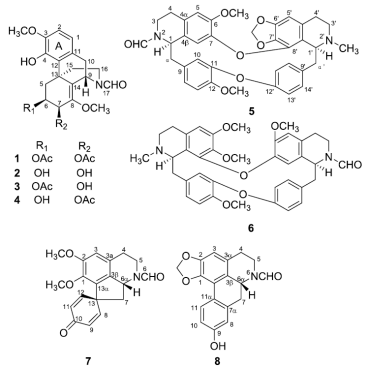
Figure 1. Structures of the alkaloids fromS. cepharantha(fromJ. Nat. Prod.).
在分离和鉴定这类化合物的过程中,作者利用1H-NMR、13C-NMR、HSQC、HMBC确定了化合物的平面结构,通过1H-NMR谱中关键氢信号的偶合常数和NOESY谱相关信号确定了其相对构型(Figure 2,J. Nat. Prod., DOI: org/10.1021/acs. jnatprod.9b00483),采用ECD结合计算拟合的方法确定了它们的绝对构型(Figure 3,J. Nat. Prod., DOI: org/10.1021/acs.jnatprod.9b00483)。

Figure 2. Key NOESY (↔) correlations in compounds1-6(fromJ. Nat. Prod.).
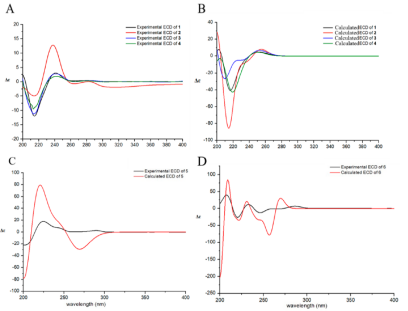
Figure 3. Experimental ECD spectra of1-4(A); ECD spectra of1-4calculated for 6S,7S,9R,13S(B); experimental and calculated (for 1R,1′S) ECD spectra of5(C); experimental and calculated (for 1R,1′S) ECD spectra of6(D)(fromJ. Nat. Prod.).
在结构鉴定的过程中,作者发现化合物1-4在室温下出现立体异构化现象,主要表现在其HPLC谱图和NMR数据上。首先,在反相HPLC上出现峰裂分现象,且在正相手性柱条件下呈现峰面积1:1的两个峰(Figure 4,J. Nat. Prod., DOI: org/10.1021/acs.jnatprod.9b00483);其次,在NMR中,峰信号都是成对出现的,通过氢谱峰面积计算和碳谱峰高比较,比例约为1:1。
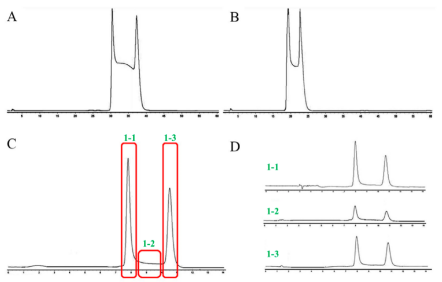
Figure 4. Revised HPLC chromatograms of1in 50% MeOH-H2O (A) and in 38% CH3CN-H2O (B). HPLC chromatogram of1from a CHIRALPAK IF chiral-phase column (Daicel CHIRALPAK IF analytic column, 4.6 × 250 mm, 4.6 μm particles, Daicel Chemical Industries, Tokyo, Japan) (C). HPLC chromatograms of various fractions of1usingn-hexane-EtOH (6:4) and a chiral-phase column (D) (fromJ. Nat. Prod.).
作者通过NMR信号对比发现,主要区别在17-N-CHO附近的氢碳信号,推测C-17处的C-N键的部分双键性使羰基不能以C-N键为轴进行自由旋转而形成异构化现象,这一推测也进一步通过NOESY谱得到确认(Figure 2,J. Nat. Prod., DOI: org/10.1021/acs.jnatprod.9b00483)。进一步采用密度泛函理论进行能量计算,对角度不同的构象转换所需能量进行计算分析(Figure 5,J. Nat. Prod., DOI: org/10.1021/acs. jnatprod.9b00483)。固定化合物其他位置构型不变,以C-N键为轴,羰基进行360°的旋转,每10°取一个构象,计算其能量值(分别在真空状态、溶剂CHCl3和DMSO中),将能量最低的构象能量定义为0 Kcal/mol,在此基础上计算其他构象能量。在真空和溶剂中,两个构象的能量势垒均小于29 Kcal/mol,解释了室温条件下异构化这一现象(旋转角度在0°和180°时,化合物处于能量最低点,此时的构象1a和1b最稳定)。
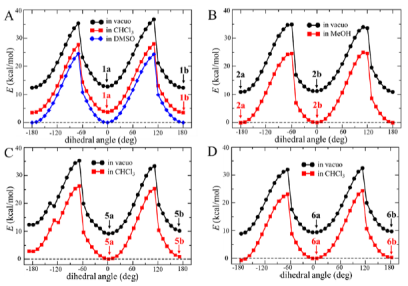
Figure 5. DFT-calculated total energies for compounds1(A),2(B),5(C), and6(D) as a function of rotation of the N−C=O group (the black, red, and blue symbols correspond to the energies of the speciesin vacuo, solvated in chloroform, and solvated in DMSO, respectively, in A, C, and D; the red symbol correspond to the energies of2solvated in methanol in B) (fromJ. Nat. Prod.).
化合物5-6的NMR信号亦是成对出现的,且化合物5异构化的比例为3:1,采用上述方法对两个化合物的异构化现象进行了能量计算分析。相似的现象也出现在化合物7-8中,造成异构化的原因亦是N-CHO的存在。在确定了新化合物异构化现象的基础上,进一步通过碳谱计算的方法对两个构象的两组核磁共振数据分别进行了准确的归属。
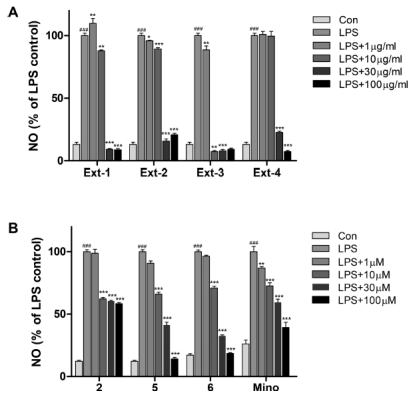
Figure 6. Anti-inflammatory activities of the extracts (A) and isolated compounds (2,5,6) (B) assayed on LPS-induced NO production in BV-2 microglial cells. Each bar represents the mean ± SE of threeindependent experiments;###p< 0.001 compared with the control group, **p< 0.01, ***p< 0.001 compared with the LPS group; Ext-1: 80% ethanol extract, Ext-2: 30% eluate, Ext-3: 70% eluate, Ext-4: 95% elutate, NO: nitric oxide, LPS: lipopolysaccharide, Mino: minocycline(fromJ. Nat. Prod.).
文章进一步对分离得到的生物碱进行体外抗神经炎症的活性评价,结果表明,化合物5(IC50, 12.0mM)和6(IC50, 12.6mM)表现出显著的抑制活性,优于阳性对照药米诺环素(IC50, 17.5mM),化合物2亦表现较显著的抑制活性,其IC50值为37.3mM。文中对活性生物碱的构效关系进行了总结(Figure6,J. Nat. Prod., DOI: org/10.1021/acs. jnatprod.9b00483)。
总结:
作者结合NMR谱图分析和TDDFT理论进行构象转化能量计算对异喹啉类生物碱中氮醛基异构化现象的谱图特征和异构化比例变化进行了深入探讨,从而确定了化合物的绝对构型,该方法对解决这类生物碱的立体构型问题提供了思路。此外,利用LPS-诱导的BV2小胶质细胞异常活化的筛选模型,以NO释放量为评价指标,对单体化合物的抗神经炎症活性进行评价,提示该类化合物为潜在的抗神经炎症抑制剂。该工作以“Amide-iminoateisomerism inanti- neuroinflammatoryisoquinolinealkaloids fromStephania cepharantha”为题发表在J. Nat. Prod.(DOI: org/10.1021/acs.jnatprod.9b00483)上,第一作者为沈阳药科大学肖姣博士和宋俊玉硕士。通讯作者为沈阳药科大学李宁教授和陈刚副教授(论文作者:Jiao Xiao, Junyu Song, Bin Lin, Wei Li, Yanqiu Yang, Jingyu Liu, Yue Hou, Gang Chen*,and Ning Li*)。