近日,我校无涯创新学院孙进教授、孙丙军教授团队在白蛋白纳米递药系统的理性设计与抗肿瘤应用研究方面取得重要进展,通过精准调控烷基链长度与连接键化学特性,成功构建了兼具高效抗肿瘤活性与良好安全性的阿霉素前药白蛋白纳米粒。相关研究成果以“Optimizing doxorubicin prodrug albumin nanoparticles through tailored alkyl chain lengths and optimized linker chemistry”为题发表于国际纳米领域期刊《Nano Today》。
阿霉素(DOX)是临床应用广泛的蒽环类化疗药物,对乳腺癌、卵巢癌、白血病等多种恶性肿瘤具有显著疗效,但其非特异性分布导致的心脏毒性和骨髓抑制等不良反应极大限制了其临床应用。人血清白蛋白(HSA)因免疫原性低、生物相容性好且具有天然肿瘤靶向性的优势,成为理想的药物载体。但阿霉素与HSA的低亲和力导致白蛋白纳米粒的粒径不均、稳定性差,难以实现高效递药。
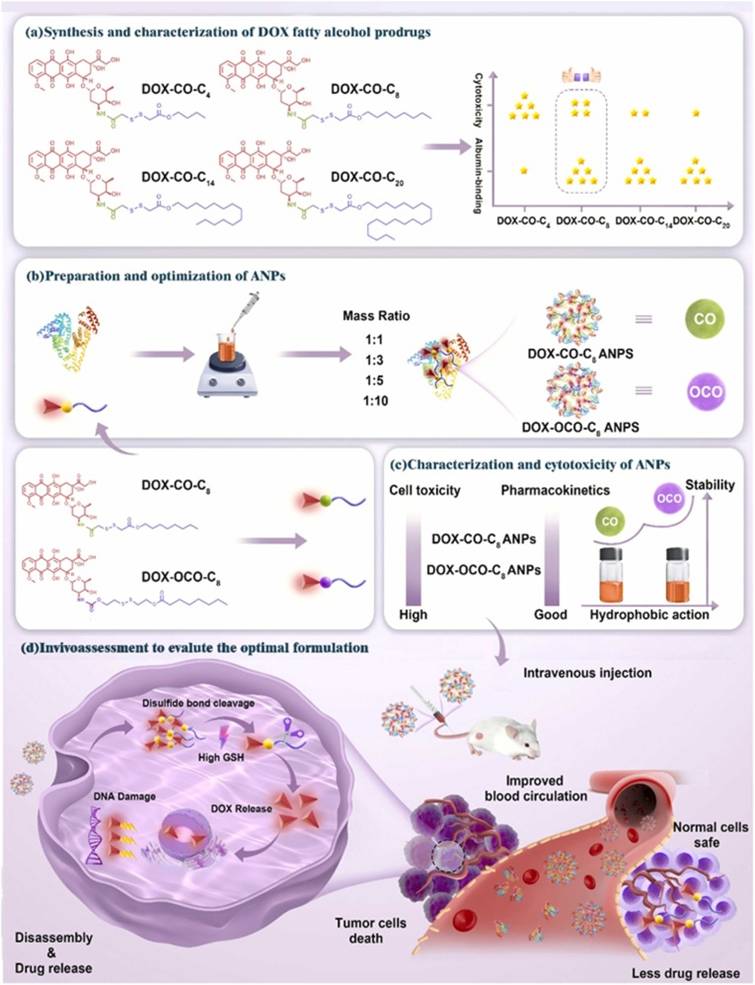
针对上述核心难题,研究团队提出了“前药结构精准调控-白蛋白组装优化-肿瘤微环境响应释放”的一体化设计策略。首先合成了碳链长度分别为C4、C8、C12、C20的酰胺键连接型阿霉素-脂肪醇前药,系统探究了烷基链长度对前药与HSA结合亲和力的影响。发现当碳链长度为8个碳原子时,前药与HSA的结合亲和力最强,可形成包封率超92%的稳定白蛋白纳米粒。但进一步研究发现,酰胺键的化学稳定性过高,导致前药在肿瘤细胞内无法有效释放活性阿霉素,细胞毒性显著减弱。为解决药物释放不足的问题,团队创新性地将稳定的酰胺键替换为具有更高反应活性的氨基甲酸酯键,构建了新型还原响应型前药DOX-OCO-C8。该前药不仅保持了与HSA的强结合能力,还实现了肿瘤细胞内的精准药物释放:在肿瘤细胞高浓度谷胱甘肽的还原环境下,二硫键断裂后暴露的巯基可与氨基甲酸酯键发生分子内亲核取代反应,快速释放出完整的活性阿霉素。优化后的DOX-OCO-C8白蛋白纳米粒具有优异的制剂稳定性,药代动力学性质显著改善,肿瘤靶向性增强,并且治疗窗口大幅拓宽。在20mg/kg的高剂量下,其抗肿瘤疗效与临床常用的阿霉素脂质体(Doxil)相当,且未观察到明显的体重下降、肝肾损伤及骨髓抑制等全身毒性,而同等剂量的游离阿霉素会产生致命的毒副作用。
该研究系统阐明了烷基链长度和连接键化学特性对白蛋白纳米粒组装、体内行为及抗肿瘤疗效的调控规律。这一成果不仅为解决阿霉素化疗中“疗效与毒性难以平衡”的难题提供了全新解决方案,也为其他亲水或两亲性药物的白蛋白递药系统设计提供了重要的理论指导和技术支撑。
我校2022级硕士研究生房红锴、2020级博士研究生张璟璇为论文共同第一作者,孙进教授和孙丙军教授为共同通讯作者,沈阳药科大学为第一通讯单位。该研究得到了国家重点研发计划、辽宁省教育厅青年创新团队、辽宁省“兴辽英才计划”及辽宁省重点研发计划等项目的资助。
原文链接:https://www.sciencedirect.com/science/article/pii/S1748013226000617?via%3Dihub