近年来,驱动患者免疫系统对抗肿瘤的免疫疗法取得了很大的进展。然而,当前免疫治疗的效果在针对三阴性乳腺癌症(TNBC)时受到免疫抑制微环境的阻碍,其典型特征是T细胞浸润不足和免疫原性低。最近,越来越多的光疗和纳米技术研究集中于影响免疫系统以治疗肿瘤。光疗,包括光动力疗法(PDT)和光热疗法(PTT),在免疫治疗中引起了越来越多的关注,因为它创建了肿瘤相关抗原(TAA)库,并有助于树突状细胞(DC)成熟。尽管如此,局部光疗的单一疗法不足以唤起强大而持久的肿瘤免疫原性来抑制肿瘤转移和复发,迫切需要将光疗和免疫刺激策略相结合,以实现免疫原性差的TNBC的光免疫疗法的协同治疗效果。
为此,我校孙进教授课题组揭示了气体治疗激活cGAS-STING通路的免疫佐剂特性,并有效增强了聚集诱导发光体材料(AIEgen)针对免疫原性差的TNBC的光免疫治疗效果。在这项工作中,课题组构建了GSH/NIR顺序启动的气体纳米佐剂,联合AIEgen介导的PDT/PTT协同治疗和肿瘤特异性放大的H2S/CO/Mn2+释放,以有效侵入肿瘤细胞,并显著激活cGAS-STING通路,用于低免疫原性TNBC的治疗。具体地,课题组设计了四硫键桥联的病毒状空心介孔二氧化硅(tvHMS)用于负载AIEgen和羰基锰(MnCO)以制备气体纳米佐剂(MTHMS)(图1a)。当气体纳米佐剂在肿瘤部位蓄积后,病毒状表面帮助其更有效地被肿瘤细胞摄取。在进入肿瘤细胞后,过度表达的GSH可以破坏四硫键,引发MTHMS的解体,从而导致肿瘤特异性和可控的药物释放,并通过消耗GSH放大PDT治疗,同时释放出H2S气体。在近红外光照射下,基于AIEgen的PDT/PTT协同疗法可以原位激活MnCO前药,产生Mn2+和CO。H2S和CO将引起肿瘤细胞的线粒体功能障碍,诱导线粒体DNA(mtDNA)的细胞内释放,激活cGAS-STING通路,发挥免疫佐剂特性。此外,Mn2+是一种强大的cGAS激动剂,可增强肿瘤细胞和DC中STING介导的I型干扰素反应。之后,IFN-β的表达水平显著提高,有助于DC成熟,并启动抗肿瘤T细胞反应(图1b)。相关研究成果发表在Nature Communications,文章题目为“Gas therapy potentiates aggregation-induced emission luminogen-based photoimmunotherapy of poorly immunogenic tumor through cGAS-STING pathway activation”。
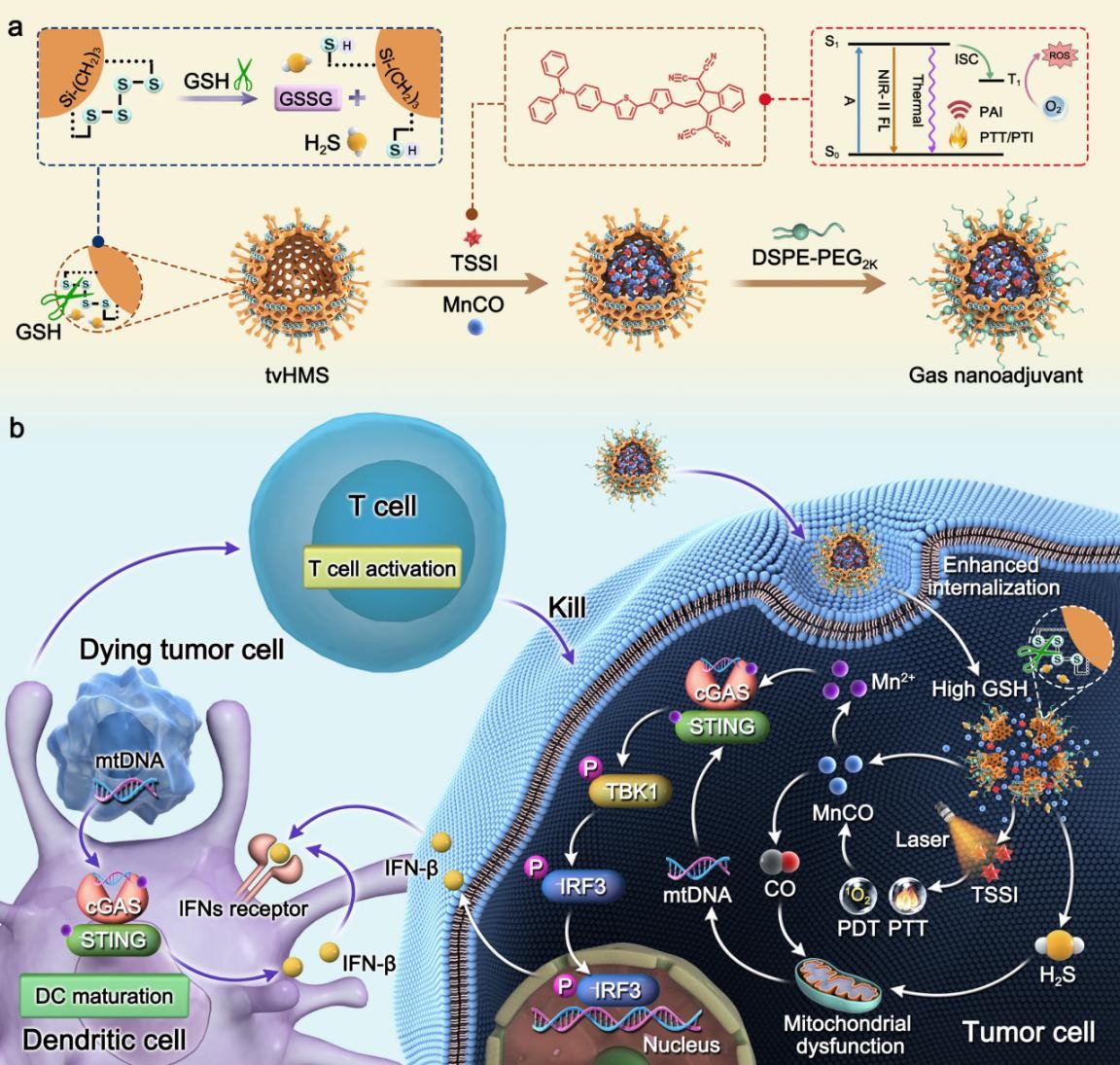
图1.气体纳米佐剂制备与起效机制示意图
该研究将基于AIEgen的光疗和气体介导的cGAS-STING通路激活的免疫刺激策略整合到气体纳米佐剂中,为开发针对免疫原性差的肿瘤的光免疫疗法提供了新的思路。
我校和新加坡国立大学联合培养博士研究生王开元、中国科学院福建物质结构研究所李阳副研究员和我校博士研究生王霞为共同第一作者,无涯创新学院孙进教授、新加坡国立大学陈小元教授、深圳大学王东教授、浙江海洋大学周英棠教授为共同通讯作者,我校为第一通讯单位。该研究得到了何仲贵教授的指导与支持,获得了国家重点研发计划和国家自然科学基金的资助。
原文链接:https://doi.org/10.1038/s41467-023-38601-7