我校药学院乔明曦教授和陈大为教授研究团队基于肿瘤细胞异常脂肪酸代谢行为,通过正反馈机制调节细胞内脂肪酸氧化代谢介导ROS持续生成,所诱发的免疫原性细胞死亡效应可有效协同免疫检查点抑制疗法,显著增强体内抗肿瘤疗效。相关科研成果“Self-amplified ROS production from fatty acid oxidation enhanced tumor immunotherapy by atorvastatin/PD-L1 siRNA lipopeptide nanoplexes”发表于国际纳米材料领域权威期刊Biomaterials(IF: 15.304,DOI: 10.1016/j.biomaterials.2022.121902)。

ROS作为一种重要的肿瘤治疗手段不仅可以直接产生肿瘤细胞杀伤作用,还可以诱导肿瘤细胞产生免疫原性细胞死亡,与免疫治疗发挥协同抗肿瘤作用。传统的ROS生成策略如光动力(PDT)和化学动力(CDT)面临氧化底物匮乏所致的ROS生成效率低、不可持续等困境。针对乏氧、缺少营养物质供应的肿瘤微环境环境,肿瘤细胞对自身的脂肪酸(FA)代谢进行重编程,上调FA从头合成,增强外源性FA摄取。同时,为了避免脂毒性和氧化损伤,下调脂肪酸氧化代谢(FAO)水平,将过量的FA转化成甘油三酯(TG)储存。基于肿瘤细胞异常的脂肪酸代谢机制,团队在前期研究成果(Biomaterials 2021, 271:120711; Biomaterials 2018, 162:47-59;ACS Applied Materials & Interfaces 2019, 11 (18): 16296-16310 16310; Biomaterials 2014, 35:9877-9887)的基础上设计并合成了一种pH/还原性双敏感的两亲性脂肽(C18-pArg8-ss-pHis10),用于PD-L1 siRNA和阿托伐他汀(Ato)的共递送。载药脂肽纳米复合物响应内涵体/溶酶体弱酸性和还原性环境,触发Ato和siRNA的快速解离,并高效介导药物的内涵体/溶酶体逃逸。
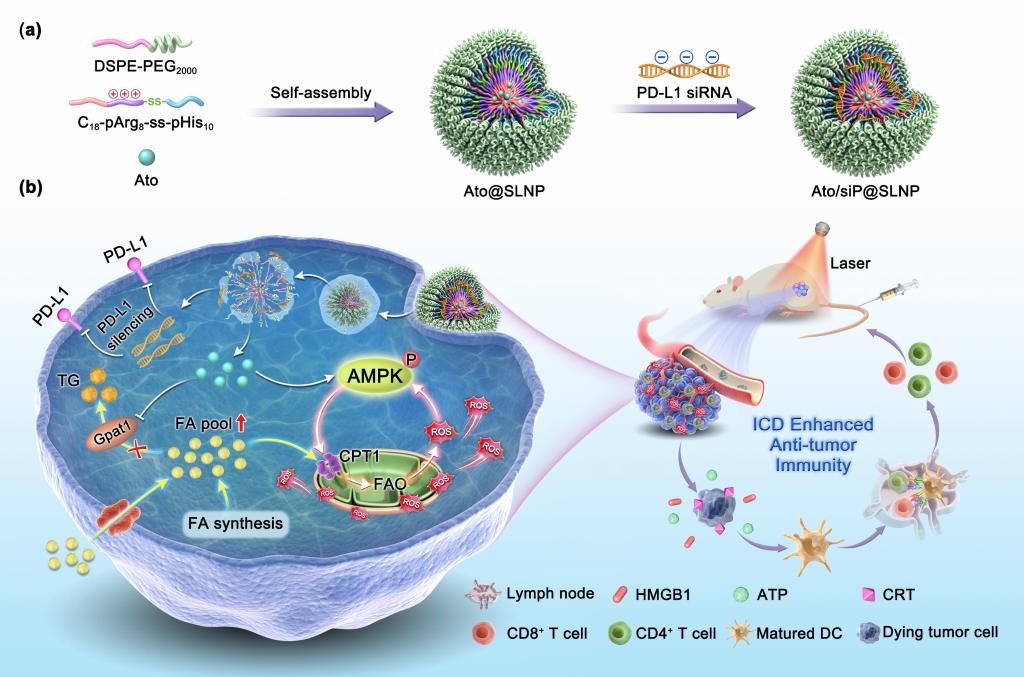
进入细胞浆中的Ato通过磷酸化方式激活AMPK-CPT1通路,上调细胞内脂肪酸氧化(FAO)代谢过程,促进细胞内ROS的生成。所生成的ROS可反馈性地激活AMPK,形成AMPK/FAO/ROS正反馈循环机制。同时,Ato可激活PKA-Gpat1通路,抑制脂肪酸向甘油三酯转化,为FAO提供氧化分解底物维持其激活状态和ROS的持续生成。生成的ROS可有效诱导ICD效应,促进免疫细胞向肿瘤组织浸润。协同PD-L1 siRNA解除免疫抑制作用增强体内抗肿瘤疗效。本研究基于肿瘤细胞的异常脂肪酸代谢,提出一种全新的自增强、持续生成ROS策略,并验证了其对免疫疗法的协同增强作用,为基于ROS的肿瘤治疗策略及免疫治疗提供了新的研究思路和依据。
我校博士研究生高岩为论文第一作者,药学院乔明曦教授和陈大为教授为共同通讯作者。该研究得到了国家自然科学基金、沈阳市中青年科技创新人才支持计划的资助。
文章连接:https://doi.org/10.1016/j.biomaterials.2022.121902