近日,国际化学领域知名期刊Organic Letters(IF=6.072)在线发表了我校制药工程学院陈国良教授课题组在铜催化方法学研究领域的最新研究成果,论文题目为“Copper-Catalyzed Oxidative C−C Bond Cleavage of Alkyl-(Hetero)arenes Enabling Direct Access to Nitriles”。
有机腈是一类广泛存在于药物分子、农用化学品、功能性材料以及天然产物中的化合物,由于其较高的反应活性常常被用作合成酰胺、酸、醛和环状化合物的前驱体。传统的有机腈合成方法主要包括Sandmeyer反应、过渡金属催化腈化以及碳氢键的直接氰基化,这些方法都存在一些限制性因素,如预官能团化起始原料、需使用毒性试剂或者无机氰化物以及需要化学计量的金属试剂参与等。因此,发展一个可持续性且绿色环保的直接生成有机腈的方法具有非常重要的意义。
芳基烷烃类化合物作为一类价格低廉且工业储量丰富的不饱和碳氢资源,已经有许多方法致力于将其转化芳基腈,但是该方法具有一些缺点,如过度依赖化学计量及环境不友好的氧化剂、采用爆炸性叠氮化物(如NaN3)、不稳定的氮源(TBN)以及较窄的底物范围和剧烈的反应条件等,使其应用受到限制。
研究发现,采用CuOAc作为催化剂、尿素作为氮源、无水碘化锂作为添加剂,在氧气存在下可以将各类烷基取代的芳香类化合物转化为相应的有机腈产物。该方法底物适用性广泛,官能团耐受性良好,并且对于敏感性官能团如对甲苯磺酸基、酯基等的存在均能以良好的收率得到相应的腈。此外,对于一些长链取代的烷基芳烃,该方法也能以良好的选择性和收率得到相应的腈。此外,对于一些烷基取代的芳杂环类化合物,该方法同样适用。通过克级反应和混合底物实验进一步证明了该方法的普适性。
通过控制实验以及自由基抑制实验对反应机理进行了探究,结果表明该反应是由碘离子促进的自由基串联式反应。对于二级碳和三级碳中心型底物,我们结合之前文献报道提出了极具新颖性的反应机理。
综上所述,以CuOAc为金属催化剂、尿素为氮源、碘化锂为添加剂、氧气为氧源的反应体系可以实现各类烷基取代的芳环及芳杂环型底物转化为有机腈类产物,为不饱和碳氢资源的转化和有机腈的合成提供了一种高效、绿色且条件温和的新方法。
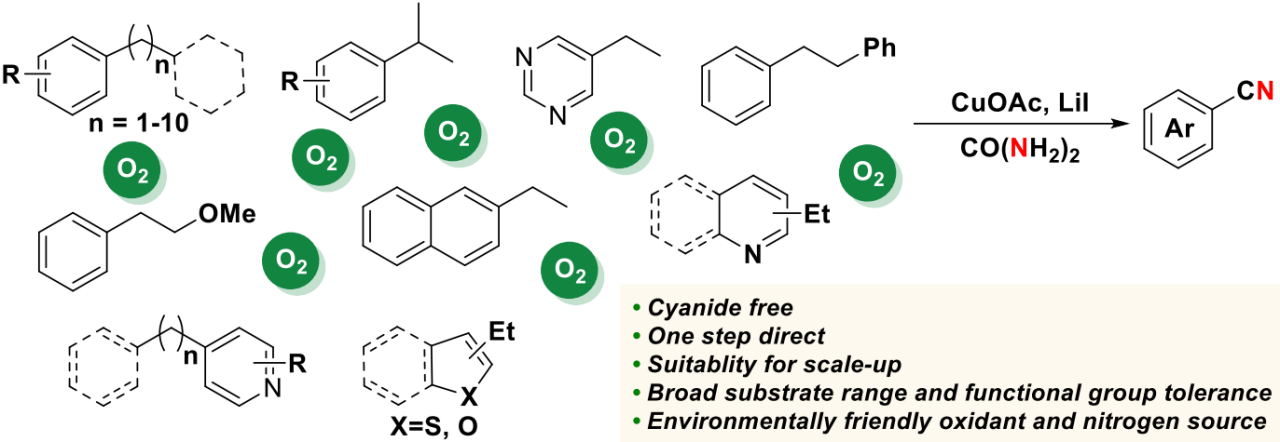
图1. CuOAc催化烷基取代的芳环及芳杂环底物发生碳碳键氧化断裂氰基化
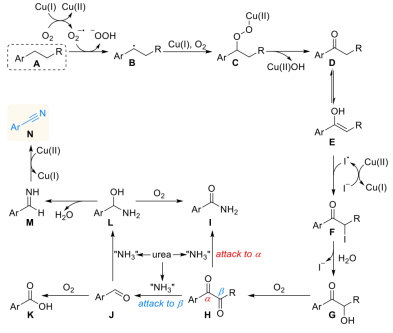
图2. 可能的反应机理
我校制药工程学院2019级硕士研究生薛盖君为论文第一作者,制药工程学院陈国良教授和中国科学院大连化学物理研究所戴文研究员为共同通讯作者。
文章链接:https://pubs.acs.org/doi/pdf/10.1021/acs.orglett.2c02238