我校药学院王思玲教授课题组多年来致力于难溶性药物纳米递送系统的研究,主持的“纳米逆晶载药骨架技术用于难溶性药物给药系统的设计与评价”的研究获得辽宁省自然科学二等奖。该项目围绕着难溶性药物的口服生物利用度低与注射给药靶向效率差的科学难题,对难溶性药物给药系统进行了深入系统的研究,并已取得重要的科学发现与开拓创新性成果。相关研究成果已发表SCI论文50余篇,授权中国发明专利6项,项目的8篇代表性论文发表在J. Control. Release和Biomaterials等本领域国际权威期刊上,8篇代表性论文的总IF为56.716,SCI他引554次,单篇最高引183次,其中有2篇入选ESI前1%高被引论文,同时被Web of Science评为高被引论文;相关成果被Chem Rev(IF= 47.928)和Chem Soc Rev (IF=38.618) 等国际著名学术期刊评论和重点介绍。
在创新药物应用中,约有40%以上的药物为水难溶性药物,且其中高达70%的药物由于溶解度不足导致难溶性药物的生物利用度低与靶向效率差,进而难以用于临床或不能发挥良好的疗效,课题组紧紧围绕着新药创制和现有药物功效改善亟需解决的科学难题,创新提出“逆晶载药”新概念,以“逆晶载药”设计的纳米骨架用于分散与装载难溶性药物构建新型载药系统,相关研究已基本形成完整的科学体系,包括:难溶性药物骨架载体的设计与构建,难溶性药物骨架载药的速释、缓释与控释给药系统,难溶性药物骨架载药系统的靶向递送及相关系统形成的药剂学基础。研究团队在设计与构建新型纳米骨架给药系统并揭示其作用机理方面取得的重要的科学发现为:
(1)创新提出“逆晶载药”的新概念,①根据药物晶体形成的晶胞参数设计骨架载体的孔道特征,该特征为可破坏或可阻断药物晶体的形成,称“逆晶型”;②根据药物析晶形态状设计骨架载体的孔道特征,该特征为可破坏或可干扰药物晶体的形态形状,称“逆晶形”。并已阐明以新概念设计构建的新型给药系统促进难溶性药物生物利用度显著提高的作用机制;以新概念设计新载体并获得新型骨架载药系统的新思路,为深入研究骨架类新辅料与丰富临床制剂的新品种提供了技术平台与理论指导(如图1为逆晶载药骨架技术构建的部分骨架载体的电镜下形态)。

图1 多种骨架载体于SEM和TEM下的形貌:纳米球外形(a)和内部结构(b)
(2)发现通过调整骨架结构并结合高分子包衣技术,难溶性药物载药体系于特定生理条件下的释药特征可分别呈现速释、缓释与控释的动力学规律(见图2)。该释药动力学规律的发现,为后续类同载体的研究提供重要的理论指导,为丰富药剂学的缓控释制剂的基本理论与促进新型材料分支学科的形成提供了重要的实验依据。
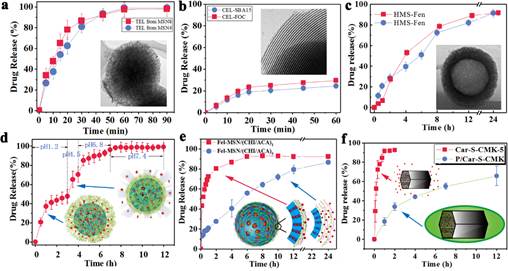
图2 难溶性药物载药体系于特定生理条件下的释药特征分别呈现速释(a, d)、缓释(b, e, f)与控释(c)的动力学规律
(3)发现以“生理响应性开关”修饰骨架载体,由于特定或病变组织生理条件的改变,使难溶性药物载药系统的“开关”脱落或打开,骨架释放药物,能够实现药物于特定部位的靶向递送(见图3)。该发现为解决难溶性药物的靶向效率差与毒副作用大的科学难题提供了创新性的探索思路与重要的科学依据。

图3 骨架载体的载药、靶向递送与敏感型释药过程(a)及不同“生理响应性开关”修饰的载药系统于靶部位分别呈现还原与酶(b)、还原(c)和pH (d) 敏感释药特征