近日,美国化学会旗下期刊ACS Nano(IF = 15.8)在线发表了我校药学院唐星/苟靖欣课题组在口服多肽研究领域取得的最新研究成果,论文题目为“Milk Exosome−Liposome Hybrid Vesicles with Self-Adapting Surface Properties Overcome the Sequential Absorption Barriers for Oral Delivery of Peptides”。
由于强酸和蛋白酶环境下的降解,黏液层的捕获,小肠上皮细胞的不相容特性以及“入胞容易出胞难”的低效率基底侧胞吐等多重胃肠道屏障,开发多肽药物口服递送系统仍然是一项艰巨的挑战。牛奶外泌体(mExos)因其出色的跨上皮屏障能力,已展现出作为蛋白和多肽类药物口服递送载体的巨大潜力。然而,天然mExos载体在口服递送过程中仍然面临着诸如黏液层的穿越能力有限、药物包封效率较低以及膜蛋白在胃肠道环境中的稳定性较差的挑战。这些问题阻碍了天然mExos在口服多肽递送领域的进一步应用。
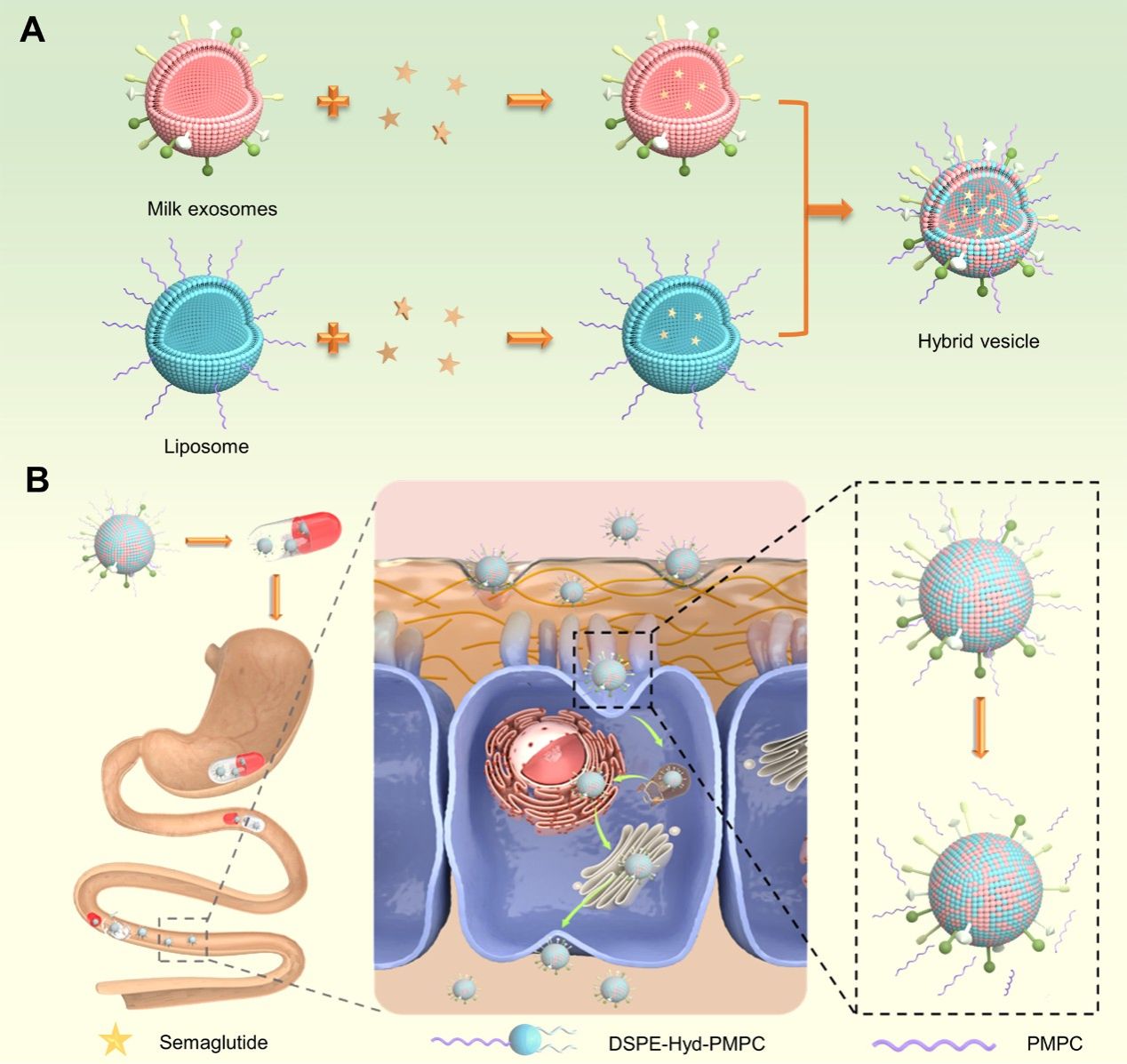
在该研究中,课题组通过将新型功能化脂质体与天然mExos融合,设计了一种具有自适应表面特性的杂化囊泡(mExos@DSPE-Hyd-PMPC),克服了天然mExos的局限性,充分释放其在口服多肽递送中的潜力。通过在高度亲水的两性离子聚合物(PMPC)和磷脂之间引入pH敏感的腙键(Hyd),并利用空肠表面的pH微环境,实现了mExos@DSPE-Hyd-PMPC的表面性质转变。在空肠肠腔中,mExos@DSPE-Hyd-PMPC的强水化层和中性电荷表面属性表现出优秀的膜蛋白保护效果和有效的黏液层穿透效果。在到达空肠上皮细胞表面后,杂化囊泡表面亲水层智能响应脱落,高度保留的膜蛋白和正电荷表面的更有效地克服了小肠上皮细胞顶膜屏障、细胞内运输屏障和基底外侧胞外分泌屏障。与天然mExos相比,杂化囊泡将索马鲁肽的包封率提高2.4倍,其自适应表面特性提高口服生物利用度2.0倍(达8.7%),并显著增强了药物的治疗效果。该研究为天然mExos口服应用的合理设计提供了新见解,为口服多肽克服层序吸收障碍提供了一种有效范例。
我校2021级博士研究生肖佩夫、王翰洵为论文共同第一作者,药学院唐星教授、苟靖欣副教授为共同通讯作者,沈阳药科大学为第一通讯单位。该项研究得到了国家自然科学基金(No. U22A20384、No. 82204298)项目的支持。
文章链接:https://doi.org/10.1021/acsnano.4c02560